ルセンティス 臨床成績に関して
本剤は国内臨床試験及び外国臨床試験成績を基に評価され承認されました。そのため紹介する臨床試験には、一部承認外の試験成績が含まれています。
| 「禁忌を含む使用上の注意」はこちらをご参照ください。 |
レーザー光凝固療法を対照とした第Ⅲ相比較検証試験
(REVEAL試験:D2303 試験)1,2)
投与開始1〜12ヵ月後における最高矯正視力スコアのベースラインからの期間平均変化量(主要評価項目)
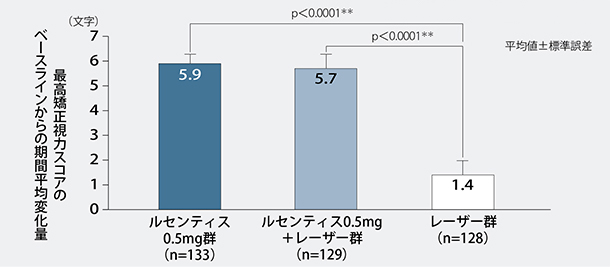
投与開始1~12ヵ月後における最高矯正視力スコアのベースラインからの期間平均変化量は、ルセンティス0.5mg群、ルセンティス0.5mg+レーザー群、レーザー群で、それぞれ5.9、5.7、1.4文字の増加でした。
ルセンティス0.5mg群、ルセンティス0.5mg+レーザー群とレーザー群を比較した結果、投与開始1~12ヵ月後における最高矯正視力スコアのベースラインからの期間平均変化量はルセンティス0.5mg群、ルセンティス0.5mg+レーザー群ともレーザー群と比較して有意に増加し、レーザー群に対する優越性が検証されました(いずれもp<0.0001、両側層別化Cochran-Mantel-Haenszel検定)。
投与開始1~12ヵ月後における最高矯正視力スコア*のベースラインからの期間平均変化量
* mean value-last observation carried forward(MV-LOCF)法(欠測値の直前と直後の実測値の平均値)で補填
** 層別化Cochran-Mantel-Haenszel検定によって解析した。
安全性
副作用
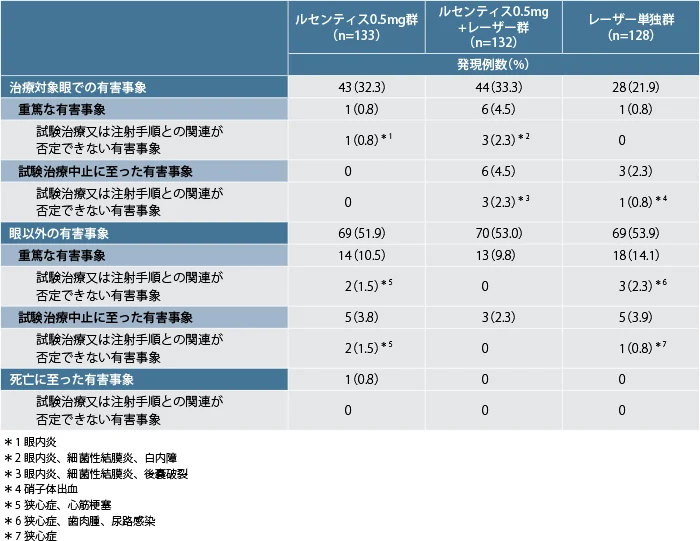
ルセンティス0.5mg群133例中29例(21.8%)、ルセンティス0.5mg+レーザー群133例中28例(21.2%)、レーザー単独群128例中18例(14.1%)に副作用が認められました。治療対象眼の副作用はルセンティス0.5mg群133例中23例(17.3%)、ルセンティス0.5mg+レーザー群132例中25例(18.9%)、レーザー単独群128例中13例(10.2%)に認められ、主な副作用はルセンティス0.5mg群及びルセンティス0.5mg+レーザー群では結膜出血(それぞれ13例(9.8%)及び12例(9.1%))、硝子体浮遊物(それぞれ4例(3.0%)及び6例(4.5%))などでした。レーザー単独群では、結膜出血7例(5.5%)、眼充血、角膜びらん各2例(1.6%)などでした。眼以外の副作用はルセンティス0.5mg群133例中6例(4.5%)、ルセンティス0.5mg+レーザー群132例中3例(2.3%)、レーザー単独群128例中5例(3.9%)に認められ、2例以上に認められたものはルセンティス0.5mg群で糖尿病腎症が2例(1.5%)、レーザー単独群で高血圧2例(1.6%)でした。
日本人患者のルセンティス0.5mg群51例中18例(35.3%)、ルセンティス0.5mg+レーザー群52例中17例(32.7%)、レーザー単独群49例中15例(30.6%)に副作用が認められました。治療対象眼の副作用はルセンティス0.5mg群51例中13例(25.5%)、ルセンティス0.5mg+レーザー群52例中14例(26.9%)、レーザー単独群49例中10例(20.4%)に認められ、主な副作用はルセンティス0.5mg群及びルセンティス0.5mg+レーザー群では結膜出血(それぞれ9例(17.6%)及び7例(13.5%))、硝子体浮遊物(それぞれ3例(5.9%)及び6例(11.5%))などでした。レーザー単独群では、結膜出血6例(12.2%)、角膜びらん2例(4.1%)などでした。眼以外の副作用はルセンティス0.5mg群51例中5例(9.8%)、ルセンティス0.5mg+レーザー群52例中3例(5.8%)、レーザー単独群49例中5例(10.2%)に認められ、2例以上に認められたものはルセンティス0.5mg群で糖尿病腎症が2例(3.9%)、レーザー単独群で高血圧2例(4.1%)でした。- 有害事象発現率(12ヵ月)
試験方法
目 的 | 日本人を含むアジア人糖尿病黄斑浮腫(DME)患者に対するルセンティス単独治療、ルセンティス及びレーザー光凝固療法併用治療、レーザー光凝固療法単独治療の有効性を検証するとともに、安全性を検討した。 | |
| 試験対象 | DMEによる視力障害を有する日本人154例を含むアジア人患者396例(ルセンティス0.5mg群:133例、ルセンティス0.5mg+レーザー群:132例、レーザー群:131例) | |
| 試験デザイン | 第Ⅲ相、多施設共同、ランダム化、二重遮蔽、レーザー光凝固療法対照、並行群間比較試験 | |
| 投与方法 | ルセンティス0.5mg硝子体内注射又はシャム注射*1を月1回投与で開始し、投与開始3ヵ月後以降は以下の視力安定の基準を満たしていない場合は月1回の治療を継続し、満たした場合はルセンティス硝子体内注射又はシャム注射を中断した。
【ルセンティス治療の再開】 視力安定の基準を満たして治療を中断した後、DMEの進行(光干渉断層撮影法[optical coherence tomography:OCT]及び他の形態学的パラメータ、又はそのいずれかによりDMEの進行が示唆された場合)による最高矯正視力スコアの減少(悪化)が認められた場合に治療を再開し、視力安定の基準を満たすまで月1回の治療を継続した。 【レーザー(又はシャムレーザー)光凝固療法の実施方法】 投与開始1日目に実施した。ただし、初回のレーザー(又はシャムレーザー)光凝固療法は、4週間隔で2回に分けて実施可能とした。その後はETDRSガイドラインに基づいて必要と判断された場合に、3ヵ月以上の間隔をあけて実施した。 投与スケジュール Image
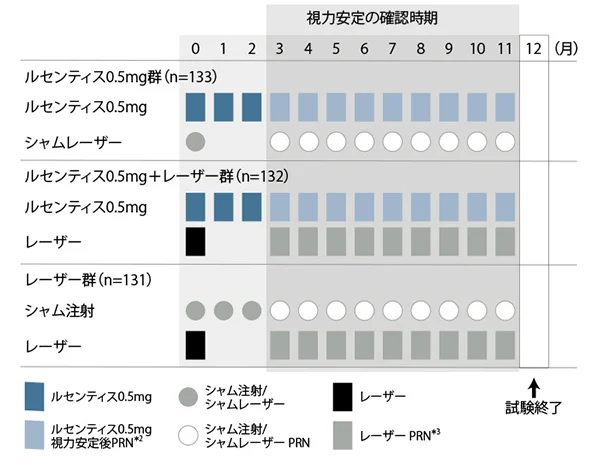
| |
| 主要評価項目 | 投与開始1~12ヵ月後における最高矯正視力スコアのベースラインからの期間平均変化量*4 | |
| 副次評価項目 | 有効性:
安全性:
| |
| 解析計画 | 有効性解析は、Full Analysis Set(FAS)集団を対象に実施した。主要評価項目における欠測データは欠測直前の実測値と欠測直後の実測値との平均値で補填するmean value-last observation carried forward(MV-LOCF)法によって補填した。副次評価項目における欠測データは、LOCF法によって補填した。優越性試験には片側仮説検定を用い、有意水準はBonferroni法又はHochberg法で補正した。各評価項目についてはDME型(局所性、びまん性)及びベースライン最高矯正視力スコア(60以下、61〜73、73超)による層別化を行い、層別化Cochran-Mantel-Haenszel検定によって解析した。安全性解析は、試験治療を1回以上受け、試験開始後に安全性評価を1回以上行った患者集団を対象に実施した。 本試験では、被験者の内訳、人口統計学的及び疾患特性、主要評価項目及び副次評価項目について、日本人部分集団のサブグループ解析を行った。 |
*1 硝子体内投与の代わりに針のないシリンジを局所麻酔下で眼球に押し付け、注射以外は同じ処置を行うこと
*2 視力安定は<視力安定の基準>参照
*3 レーザー実施方法は【レーザー(又はシャムレーザー)光凝固療法の実施方法】参照
*4 投与開始1〜12ヵ月後の12時点における最高矯正視力スコアのベースラインからの変化量の平均値
*5 中心窩を中心とする直径1mmの円内の平均網膜厚
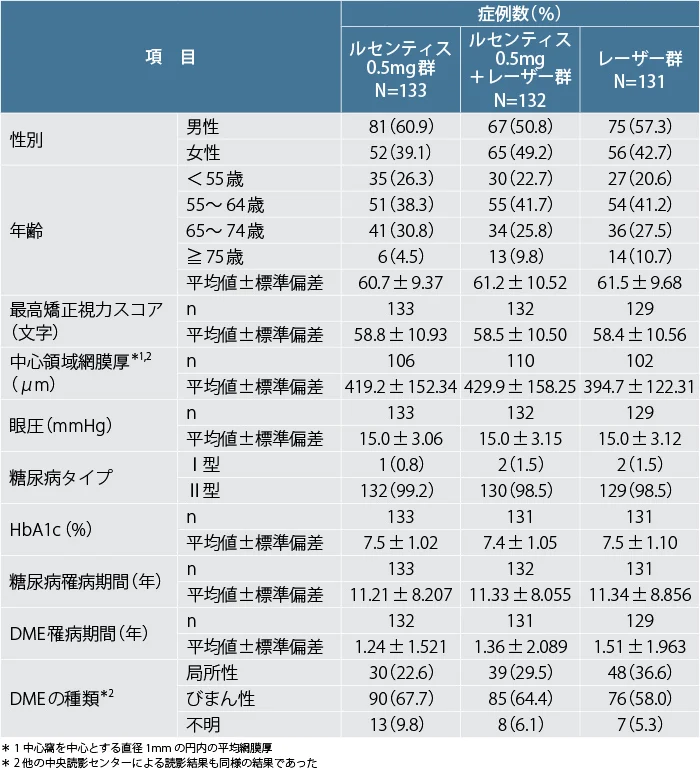
患者背景及び治療対象眼の主なベースライン特性
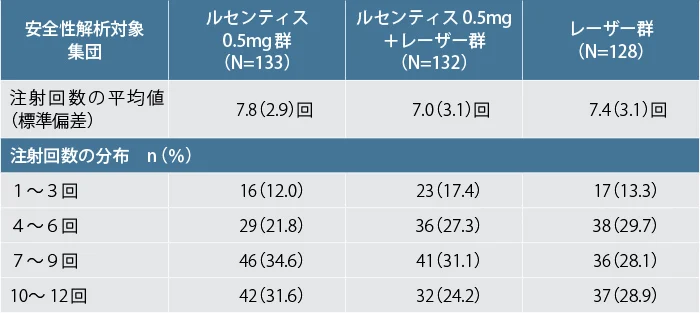
各群におけるルセンティス / シャムの注射回数
各群におけるレーザー / シャムレーザーの実施回数
1)社内資料:国際共同第Ⅲ相比較試験(D2303)[LUCU00019]承認時評価資料
2)Ishibashi T., et al.:Ophthalmology, 122(7), 1402(2015)[20160573]承認時評価資料
COI:本研究は、ノバルティスの資金により行われた。本論文の著者のうち3名は、ノバルティスの社員である。著者にノバルティスより講演料、コンサルタント料などを受領しているものが含まれる。
日本において承認されたルセンティスの用法及び用量
【糖尿病黄斑浮腫】
ラニビズマブ(遺伝子組換え)として1回あたり0.5mg(0.05mL)を硝子体内投与する。投与間隔は、1ヵ月以上あけること。
〈用法及び用量に関連する使用上の注意〉
1. 1ヵ月に1回視力等を測定し、その結果及び患者の状態を考慮し、本剤投与の要否を判断すること。
2. 投与開始後、視力が安定するまでは1ヵ月毎に投与することが望ましい。
3. 本剤による治療を開始するに際し、疾患・病態による視力等の予後を考慮し、本剤投与の要否を判断すること。
4. 定期的に有効性を評価し、有効性が認められない場合には漫然と投与しないこと。
5. 臨床試験においては、両眼治療は行われていない。両眼に治療対象となる病変がある場合は、両眼同時治療の有益性と危険性を慎重に評価した上で本剤を投与すること。なお、初回治療における両眼同日投与は避け、片眼での安全性を十分に評価した上で対側眼の治療を行うこと。
レーザー光凝固療法を対照とした第Ⅲ相比較検証試験
(RESTORE試験:D2301 試験)1)
投与開始1〜12ヵ月後における最高矯正視力スコアのベースラインからの期間平均変化量(主要評価項目)
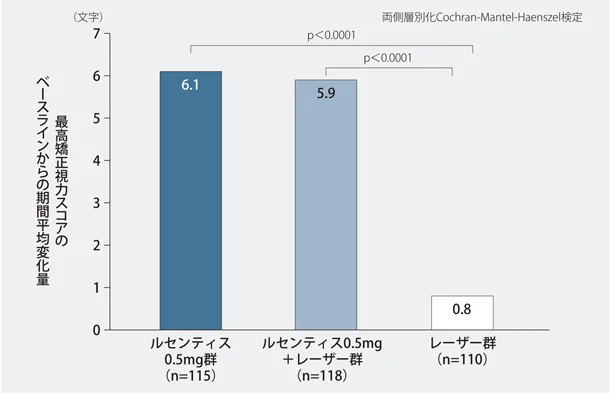
ルセンティス投与開始1~12ヵ月後における最高矯正視力スコアのベースラインからの期間平均変化量は、ルセンティス0.5mg群、ルセンティス0.5mg+レーザー群、レーザー群で、それぞれ6.1、5.9、0.8文字の増加でした。
ルセンティス0.5mg群、ルセンティス0.5mg+レーザー群とレーザー群を比較した結果、投与開始1~12ヵ月後における最高矯正視力スコアのベースラインからの期間平均変化量はルセンティス0.5mg群、ルセンティス0.5mg+レーザー群ともレーザー群と比較して有意に増加し、レーザー群に対する優越性が検証されました(いずれもp<0.0001、両側層別化Cochran-Mantel-Haenszel検定)。
投与開始12ヵ月後までの最高矯正視力スコア*のベースラインからの期間平均変化量
* mean value-last observation carried forward(MV-LOCF)法(欠測値の直前と直後の実測値の平均値)で補填
安全性
副作用
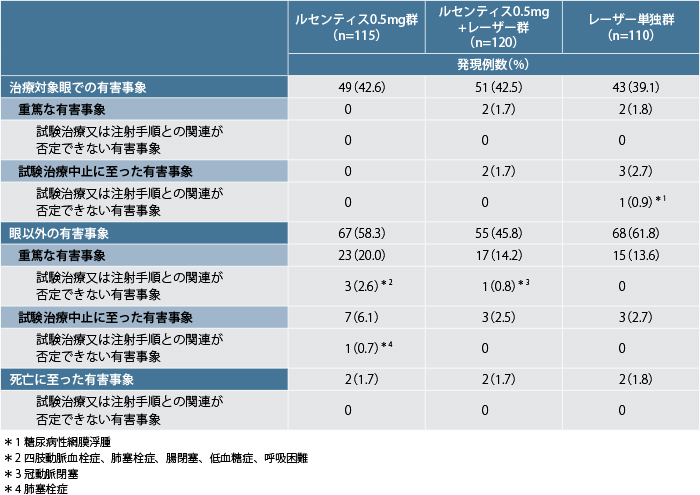
ルセンティス0.5mg群115例中37例(32.2%)、ルセンティス0.5mg+レーザー群120例中30例(25.0%)、レーザー単独群110例中22例(20.0%)に副作用が認められました。治療対象眼の副作用はルセンティス0.5mg群115例中28例(24.3%)、ルセンティス0.5mg+レーザー群120例中27例(22.5%)、レーザー群110例中20例(18.2%)に認められ、主な副作用はルセンティス0.5mg群及びルセンティス0.5mg+レーザー群では眼痛(それぞれ12例(10.4%)及び10例(8.3%))、結膜出血(それぞれ8例(7.0%)及び9例(7.5%))などでした。レーザー単独群では、眼痛11例(10.0%)、結膜充血6例(5.5%)などでした。眼以外の副作用はルセンティス0.5mg群115例中9例(7.8%)、ルセンティス0.5mg+レーザー群120例中3例(2.5%)、レーザー単独群110例中2例(1.8%)に認められ、2例以上に認められたものはルセンティス0.5mg群の肺塞栓症2例(1.7%)でした。
- 有害事象発現率(12ヵ月)
試験方法
目 的 | 糖尿病⻩斑浮腫(DME)に伴う視⼒障害を有する患者を対象にルセンティス0.5mg単独投与又はレーザーとの併用療法の、レーザー単独療法に対する優越性を検証する。 | |
| 試験対象 | DMEによる視力障害を有する患者345例(ルセンティス0.5mg群:116例、ルセンティス0.5mg+レーザー群:118例、レーザー群:111例) | |
| 試験デザイン | 多施設共同、ランダム化、二重遮蔽、レーザー光凝固療法対照、並行群間比較試験 | |
| 投与方法 | ルセンティス0.5mg硝子体内注射又はシャム注射*1を月1回投与で開始し、投与開始3ヵ月後以降は以下の視力安定の基準を満たしていない場合は月1回の治療を継続し、満たした場合はルセンティス硝子体内注射又はシャム注射を中断した。
【ルセンティス治療の再開】 視力安定の基準を満たして治療を中断した後、DMEの進行(OCT及び他の形態学的パラメータ、又はそのいずれかによりDMEの進行が示唆された場合)による最高矯正視力スコアの減少(悪化)が認められた場合に治療を再開し、視力安定の基準を満たすまで月1回の治療を継続した。 【レーザー(又はシャムレーザー)光凝固療法の実施方法】 投与開始1日目に実施した。ただし、初回のレーザー(又はシャムレーザー)光凝固療法は、4週間隔で2回に分けて実施可能とした。その後はETDRSガイドラインに基づいて必要と判断された場合に、3ヵ月以上の間隔をあけて実施した。 投与スケジュール Image
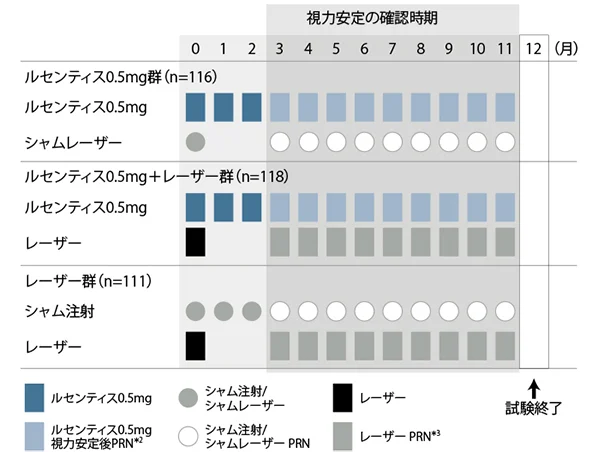
| |
| 主要評価項目 | 投与開始1~12ヵ月後における最高矯正視力スコアのベースラインからの期間平均変化量*4 | |
| 副次評価項目 | 有効性:
安全性:
| |
| 解析計画 | 有効性解析は、Full Analysis Set(FAS)集団を対象に実施した。主要評価項目における欠測データは欠測直前の実測値と欠測直後の実測値との平均値で補填するmean value-last observation carried forward(MV-LOCF)法によって補填した。副次評価項目における欠測データは、LOCF法によって補填した。優越性試験には片側仮説検定を用い、有意水準はBonferroni法又はHochberg法で補正した。各評価項目についてはDME型(局所性、びまん性)及びベースライン最高矯正視力スコア(60以下、61〜73、73超)による層別化を行い、層別化Cochran-Mantel-Haenszel検定によって解析した。安全性解析は、試験治療を1回以上受け、試験開始後に安全性評価を1回以上行った患者集団を対象に実施した。 |
*1 硝子体内投与の代わりに針のないシリンジを局所麻酔下で眼球に押し付け、注射以外は同じ処置を行うこと
*2 視力安定は<視力安定の基準>参照
*3 レーザー実施方法は【レーザー(又はシャムレーザー)光凝固療法の実施方法】参照
*4 投与開始1〜12ヵ月後の12時点における最高矯正視力スコアのベースラインからの変化量の平均値
*5 中心窩を中心とする直径1mmの円内の平均網膜厚
患者背景及び治療対象眼の主なベースライン特性
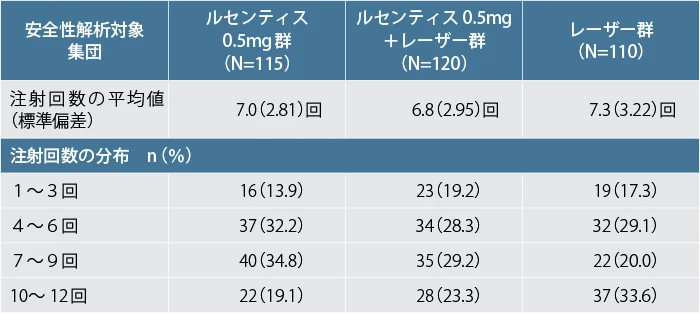
各群におけるルセンティス / シャムの注射回数
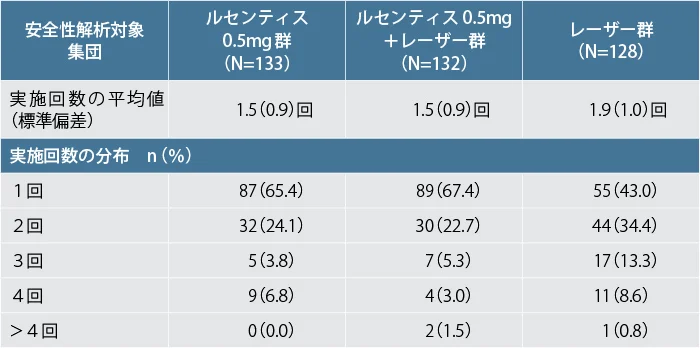
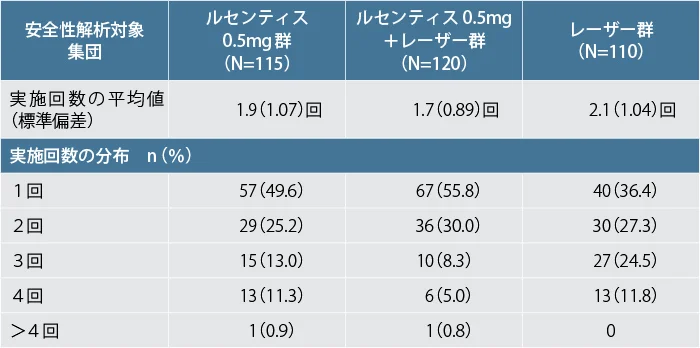
各群におけるレーザー / シャムレーザーの実施回数
1)Mitchell P., et al.: Ophthalmology, 118(4), 615(2011)[LUCM00702]承認時評価資料
COI:本研究は、ノバルティスの資金により行われた。本論文の著者のうち2名は、ノバルティスの社員である。著者にノバルティスより講演料、コンサルタント料などを受領しているものが含まれる。
糖尿病黄斑浮腫患者における第Ⅲb相長期試験
(RESTORE継続試験:D2301E1試験)1)
安全性(主要評価項目)
副作用
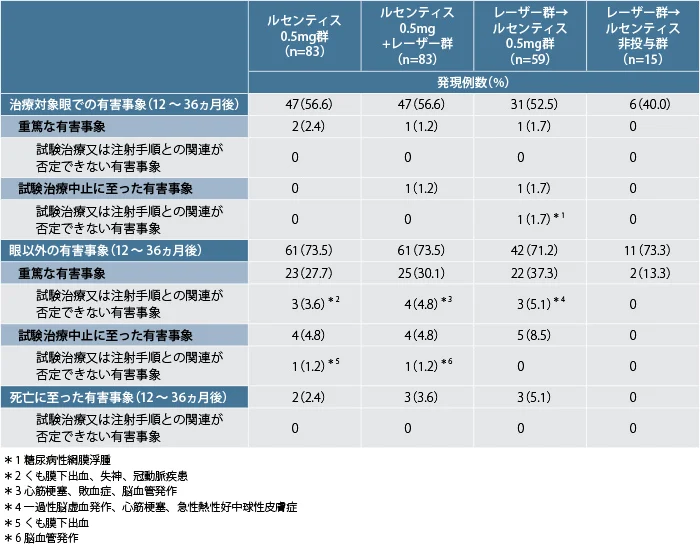
治療対象眼の副作用はルセンティス0.5mg群83例中11例(13.3%)、ルセンティス0.5mg+レーザー群83例中17例(20.5%)、レーザー群→ルセンティス0.5mg群59例中11例(18.6%)、レーザー群→ルセンティス非投与群15例中0例(0.0%)に認められ、主な副作用はルセンティス0.5mg群、ルセンティス0.5mg+レーザー群及びレーザー群→ルセンティス0.5mg群では眼痛(それぞれ8例(9.6%)、5例(6.0%)、7例(11.9%))などでした。眼以外の副作用はルセンティス0.5mg群83例中3例(3.6%)、ルセンティス0.5mg+レーザー群83例中5例(6.0%)、レーザー群→ルセンティス0.5mg群59例中3例(5.1%)、レーザー群→ルセンティス非投与群15例中0例(0.0%)に認められました。認められた副作用はルセンティス0.5mg群では冠動脈疾患、くも膜下出血、失神が各1例、ルセンティス0.5mg+レーザー群では心筋梗塞2例、脳血管発作、頭痛、敗血症各1例、レーザー群→ルセンティス0.5mg群では冠動脈疾患、皮膚疾患、脳血管発作、心筋梗塞、正色素性正球性貧血、末梢動脈閉塞症、一過性脳虚血発作各1例でした。
- 有害事象発現率(24ヵ月)
試験方法
| 目 的 | 糖尿病黄斑浮腫(DME)に伴う視力障害を有する患者を対象にルセンティス0.5mg単独投与又はレーザーとの併用療法の、レーザー単独療法に対する優越性を検証したRESTORE試験(D2301試験)の36ヵ月後の成績を検討した。 | |
| 試験対象 | RESTORE試験の治療開始12ヵ月後の評価を完了し(レーザー群も含む)、ルセンティスの治療が適切と判断されたDME患者(RESTORE試験においてレーザー群であった患者も含む)240例 | |
| 試験デザイン | 多施設共同、非遮蔽、無対照試験 | |
| 投与方法 | RESTORE試験の最終評価時(投与開始12ヵ月後)に以下のいずれかに該当した場合はルセンティス0.5mgを硝子体内注射した。(レーザー群も含む)
【ルセンティス治療の再開】 視力安定の基準を満たして治療を中断した後、DMEの進行(OCT及び他の形態学的パラメータ、又はそのいずれかによりDMEの進行が示唆された場合)による最高矯正視力スコアの減少(悪化)が認められた場合に治療を再開し、視力安定の基準を満たすまで月1回の治療を継続した。 | |
| 主要評価項目 | 安全性:眼の有害事象及び非眼科的有害事象の発現など | |
| 副次評価項目 | 有効性:
| |
| 投与スケジュール | Image
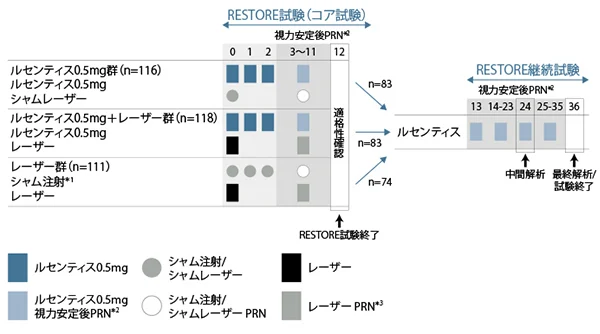
| |
| 解析計画 | 安全性解析対象集団について、コア試験のルセンティス群、ルセンティス+レーザー群及びレーザー群をコア試験終了時(12ヵ月)及び継続試験終了時(36ヵ月)に記述統計にて評価 |
*1 硝子体内投与の代わりに針のないシリンジを局所麻酔下で眼球に押し付け、注射以外は同じ処置を行うこと
*2 視力安定は<視力安定の基準>参照
*3 ETDRSガイドラインに基づいて必要と判断された場合に3ヵ月以上の間隔をあけて実施した
*4 中心窩を中心とする直径1mmの円内の平均網膜厚
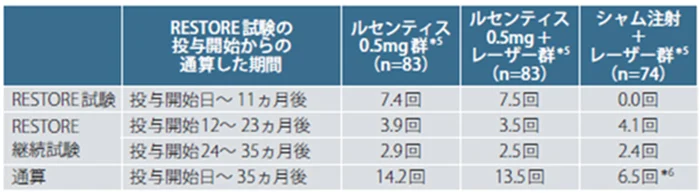
各群におけるルセンティス平均注射回数
*5 RESTORE 試験における割り付け群で表示
*6 投与開始12〜35ヵ月後における平均注射回数
1)Schmidt-Erfurth U., et al.: Ophthalmology, 121(5), 1045(2014)[LUCF00074]
COI:本研究は、ノバルティスの資金により行われた。本論文の著者のうち4名は、ノバルティスの社員である。著者にノバルティスより講演料、コンサルタント料などを受領しているものが含まれる。
日本において承認されたルセンティスの用法及び用量
【糖尿病黄斑浮腫】
ラニビズマブ(遺伝子組換え)として1回あたり0.5mg(0.05mL)を硝子体内投与する。投与間隔は、1ヵ月以上あけること。
〈用法及び用量に関連する使用上の注意〉
1. 1ヵ月に1回視力等を測定し、その結果及び患者の状態を考慮し、本剤投与の要否を判断すること。
2. 投与開始後、視力が安定するまでは1ヵ月毎に投与することが望ましい。
3. 本剤による治療を開始するに際し、疾患・病態による視力等の予後を考慮し、本剤投与の要否を判断すること。
4. 定期的に有効性を評価し、有効性が認められない場合には漫然と投与しないこと。
5. 臨床試験においては、両眼治療は行われていない。両眼に治療対象となる病変がある場合は、両眼同時治療の有益性と危険性を慎重に評価した上で本剤を投与すること。なお、初回治療における両眼同日投与は避け、片眼での安全性を十分に評価した上で対側眼の治療を行うこと。