アフィニトール NEN(神経内分泌腫瘍)の局在診断
NENの大部分は非機能性NETが占めています。それらの局在は通常のCTやMRI、US、EUSなどで診断されています。通常の癌や肉腫との鑑別はソマトスタチン受容体シンチグラフィー(SRS)が可能です。
CT
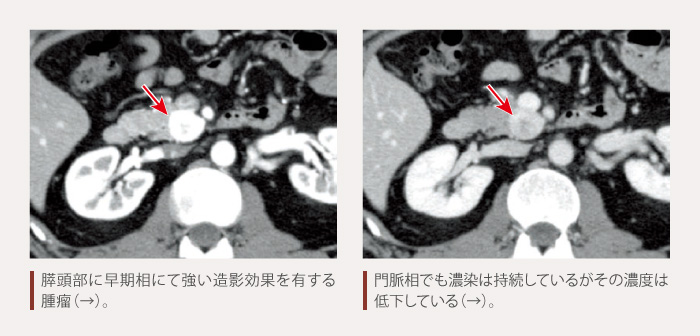
造影CTは膵NEN診断の基本となる検査です。膵NETの典型例は多血性腫瘍であり、ダイナミックCTの早期相で強い造影効果を認めます(図1)1)。CTによる肝転移などの転移巣の検出率を向上させるためには、ヨード造影剤の使用した多相性の撮像が推奨されます2)。
図1 造影CT(症例:NET G1)
MRI
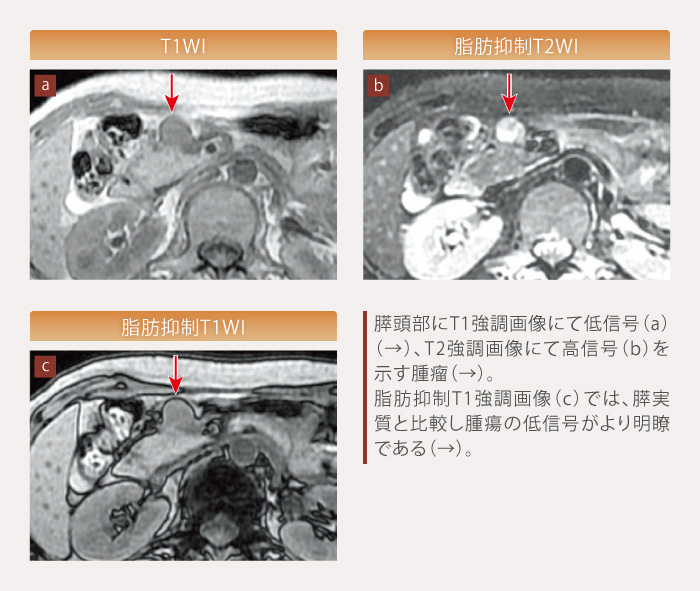
PanNETの大部分は、MRIではT1強調画像で低信号、T2強調画像で高信号として描出され(図2)1)、ダイナミックMRIでは早期相や門脈相で強い造影効果を認めます。MRIは転移巣の検出にも優れ、特に肝特異的造影剤であるGd-EOB-DTPAを用いた造影MRIによる肝転移巣の検出感度は、CTよりも良好であるとされています2)。
図2 MRI(症例:NET G1)
US
EUSはCTやMRIに比べて空間分解能が高く、微小なPanNENの診断に重要な役割を担います(図3)1)。また、EUSは消化管NETの治療方針決定のための深達度評価にも有用であり、典型例では、第2~3層を主座とする境界明瞭な低エコーの内部均一の腫瘤像を認めます(図4)1)。
図3 EUS(症例:NET G1)
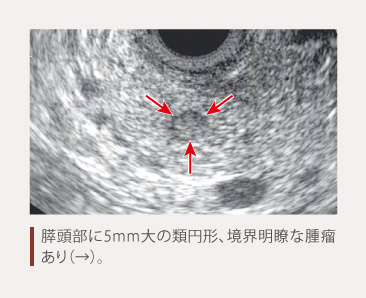
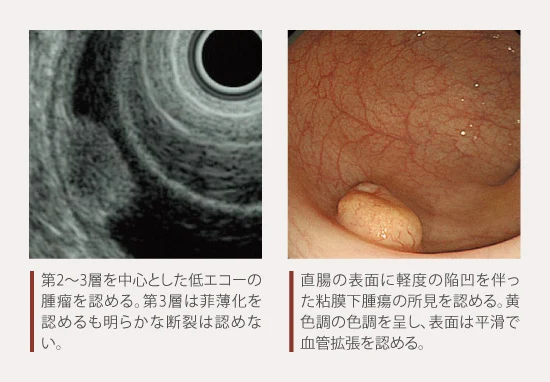
図4 EUS(症例:直腸NET)
SASI Test
直径5mm以下のNENの局在診断をする方法はSASI Testです。本邦の今村らが開発して、1987年にAnn Surg誌に発表して、現在は国際的に普及しています。1990年に米国のNIHの医師たちがいち早く追試してRadiology誌で有用性を示したのですが、彼らはSASIの原理と手技をIAS、ASVSなどと次々に改名して記載していきました。
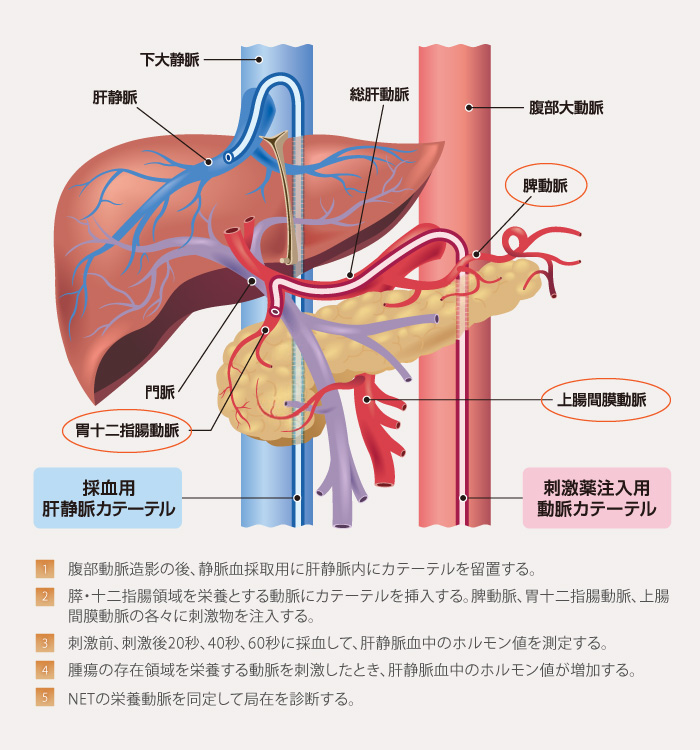
本法の原理は、膵・十二指腸領域を栄養とする動脈(脾動脈、胃十二指腸動脈、下膵十二指腸動脈)にカテーテルを挿入して、NENからのホルモン分泌を促す刺激薬、セクレチンやグルコン酸カルシウムを急速注入して、あらかじめ肝静脈に挿入しておいたカテーテルから、刺激前、刺激後20秒、40秒、60秒に採血して血中ホルモン濃度の変化を調べて、NENの栄養動脈を同定して局在を診断する方法です。この方法により、原発巣のみならず転移巣も診断できます。開腹後は触診、指診、術中USで栄養動脈の領域を精査します。本法の利点は、NENの存在しない領域を明確に診断できることであり、外科的切除領域の決定に有用です(図5)1,3)。
図5 SASI Test
 VIDEO
VIDEO
ソマトスタチン受容体シンチグラフィー(SRS)
SRSは、NETの細胞膜上に高発現するソマトスタチン受容体(SSTR)に高い親和性を示すインジウム111(111In)-ペンテトレオチド(商品名:オクトレオスキャン®)を用いたシンチグラフィです。全身の前面像・後面像に加えて断層画像(SPECT)を併用すると、病巣の検出率が向上します。
SRSは、NET原発巣および転移巣の局在診断のほか、病期診断、SSTR2の発現確認およびフォローアップの目的などでも使用されますが、SSTR低発現や1cm未満の小さい腫瘍に対しては検出能が低下することに注意が必要です。
治療方針を決める時の診断上のポイントは“肝転移があるか?”
NENの診断がついたら、治療のための検査を行います。まず何よりも肝転移や1cm以上の大きなリンパ節転移がないかどうかを調べるために、CT検査を行います。肝転移がない場合には、治癒切除術ができます。
肝転移があれば、予後は一般に悪くなります。しかし、肝転移の個数と発生部位を検討して、転移したNENをすべて外科的切除できる場合には、生存期間を延長できると考えられています。特に、肝臓の右葉や左葉に限局している場合には主病巣と共に切除することで治癒する場合もあります。NENは、膵癌や十二指腸癌などの腺癌と違って、ゆっくり増大して浸潤性も比較的弱いので、可能な限り腫瘍を少なくして、集学的治療をすることで生存期間を延長できます。90%以上腫瘍を外科的切除した上で、化学療法やTAE、TACEなどの肝動脈カテーテル法による治療を行うことが推奨されています。
機能性NENのホルモン症状に関しては、ソマトスタチンアナログにより症状の緩和効果が期待されます。
参考文献
- 今村正之 監. 膵・消化管神経内分泌腫瘍(NET)診断・治療実践マニュアル, 総合医学社, 東京, 2011
- Sundin A, et al. Neuroendocrinology. 2017; 105: 212-244
- Imamura M, et al. Ann Surg. 1987; 205: 230-239